Newsお知らせ
NMNは眼病治療に重要な潜在価値がある
加齢黄斑変性、糖尿病性網膜症、網膜脱離などの年齢に関連する眼疾患は、深刻な視覚障害や不可逆的な視力喪失につながる傾向がある。これらの疾病は、視覚を養う細胞(網膜色素上皮細胞)の細胞層から離れた目の光受容体が退化していることが特徴である。この分離は細胞死、有害な酸素分子の細胞ストレス(酸化ストレス)、炎症を引き起こす。しかし、現在のところ、光受容体の変性を治療できる薬はない。
最近、Vavvas氏とハーバード大学医学部の研究者は、ナイチンアミドモノヌクレオチド(NMN)を投与すると、網膜離脱後や酸化ストレス損傷後の光受容体を保護することができるという研究結果を『エイジング』誌に発表した。研究によると、NMNは細胞死を減少させ、目の炎症を抑制し、マウスの目の酸化ストレスに対抗する抗酸化物質のレベルを高めているという役割を果たしている。さらに、SIRT1酵素の活性の増加がこれらの保護作用を促進していることが明らかになった。研究者は論文の中で、「全体的に、研究の結果は、NMNが光受容体変性の臨床治療において潜在的な治療的価値を持っていることを示している」と述べている。
機能性細胞の鍵であるNAD+分子が眼病に重要な役割を果たす可能性がある
ニコチンアミドアデニンジヌクレオチド(NAD+)は、細胞のエネルギー産生、DNAの完全性維持、細胞増殖に重要な分子であり、眼病に重要な役割を果たす可能性がある。いくつかの研究は、酵素が眼病のメカニズムでNAD+の生成と細胞濃度に関与していることを指摘している。例えば、レバー先天性黒眼病では、NAD+の生成に重要な酵素であるNMNAT1の突然変異が発見された。さらに、NAD +の修復は、齧歯類動物の光受容体を光による網膜損傷から保護できると考えられる。
NMNは光受容体を死から守る
Vavvas氏と同僚の研究グループは、NAD+の前駆体であるNMNを用いてNAD+のレベルを上げると、網膜脱離後に光受容体を保護することが可能かどうかを調べた。この研究から、網膜脱離後のNAD +値の著しい低下はなかったが、NMNがNAD +値を通常濃度よりも高くすることがわかった。
研究者らはマウスの網膜脱離後の細胞死をTUNEL+染色と呼ばれる方法で観察した。この技術を用いて、NMNを補充することで網膜脱離後の初期の光受容体の細胞死を減少させることが発見された。マウスに250 mg/kgと500 mg/kgのNMNを投与したところ、網膜脱離24時間後に光受容体の細胞死がそれぞれ52.7%と71.0%減少したと観察した。
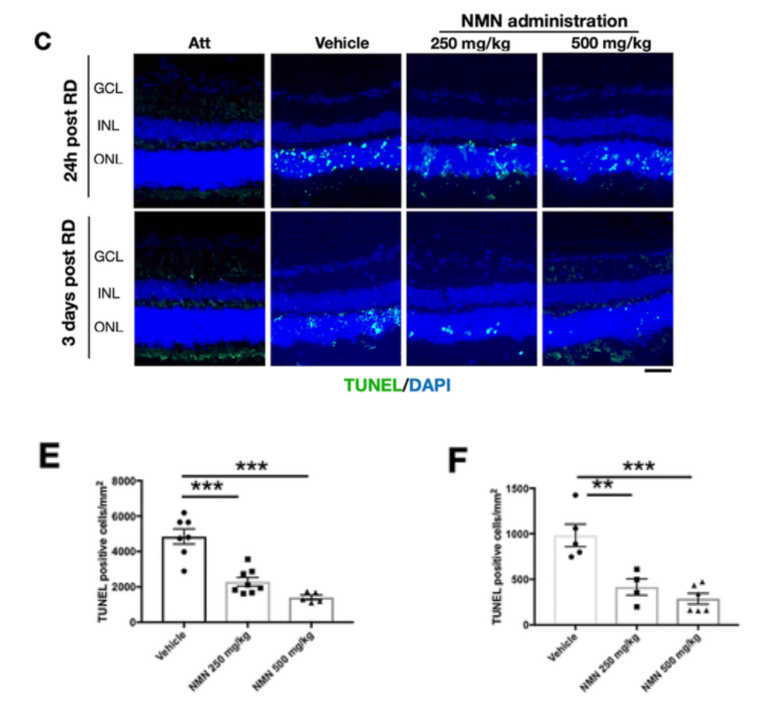
NMNは網膜脱離後の光受容体細胞死を大幅に減少させた。上図は網膜脱離後の光受容体細胞死に対するNMN治療の効果を示したものである。その上で、網膜付着(Att)、網膜剝離未処理(Vehicle)及び網膜剝離後に2種類の濃度の異なるNMN (250 mg/kgと500 mg/kg)で処理したという4つの場合の光受容体細胞の死亡数を比較した。これらの異なる条件で死滅した光受容体細胞の数を、画像(上)で陽性細胞死マーカー(緑、TUNEL)を呈する細胞を計算して調べた。左下のグラフは、1日250mg /kgと500mg /kgのNMNを24時間服用させた後に死滅した光受容体細胞の減少を示している。右下は網膜脱離のNMN治療を続けた3日後に死滅細胞数がさらに減少したことを示している。
NMNを補充することで抗酸化レベルが高まることがわかった
酸化ストレスは細胞の状態を悪化させ、光受容体細胞を死滅させるが、NMNは酸化ストレスを正常化する同時に、抗酸化剤HO-1のレベルを高めることが明らかになった。分離した網膜では、損傷を示すタンパク質成分(タンパク質カルボニルと呼ばれる)が著しく上昇し、酸化ストレスの存在を示した。しかしながら、NMN治療法は、この影響を除去する。さらに、NMNを補充すると脱落した網膜でHO-1が増加することも観察された。これらの結果は、恐らくHO-1の上昇による過剰酸化ストレスをNMNが相殺することを示唆している。
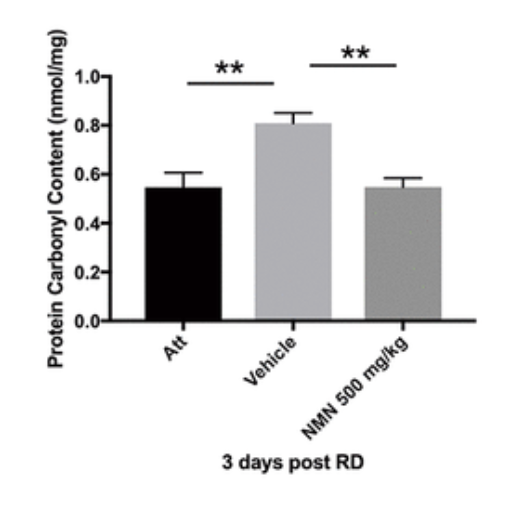
NMNを補充することで網膜脱離後の酸化ストレスを低下させ、感光体細胞を保護する。網膜脱離から3日後に酸化ストレスの指標であるタンパク質カルボニルの量が顕著にに増加したことがわかる。
抗酸化レベルの増加は、SIRT1酵素の活性にによって決まる
研究者らは、NMNが網膜脱離後の細胞保護酵素SIRT1のレベルを増加させることを発見した。これらの変化は、NAD+レベルの上昇とHO-1レベルの上昇と関連している。実際、NMNのSIRT1レベルを増加させるとHO-1が増加するが、SIRT1を減少させるとこれらの効果は相殺される。これらの研究結果は、NMNがNAD +に依存するSIRT1酵素の活性とその後のHO-1レベルを上昇させることを裏付け、また、NMNがどのようにして保護作用を発揮するかについて、独自の知見を提供している。
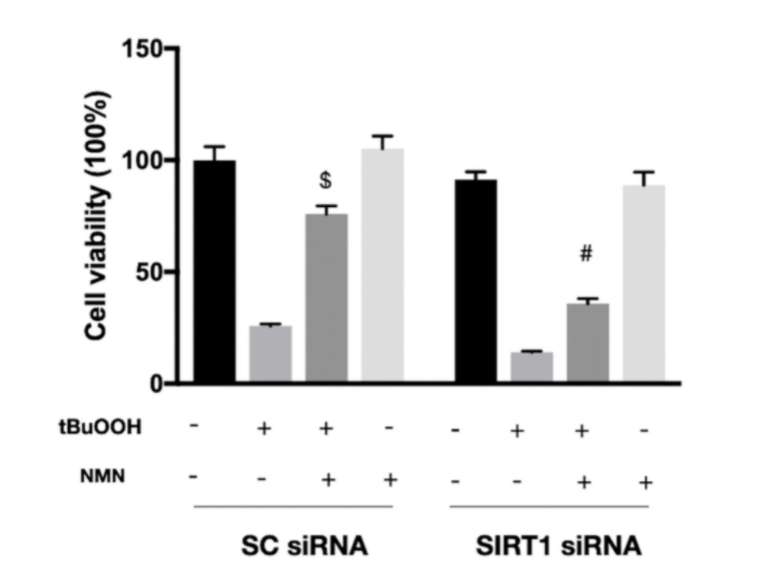
SIRT1の減少は、NMNが酸化ストレス後に発揮する保護効果を低下させる。tbuoohによって引き起こされる酸化ストレスは細胞の生存率(細胞の活力)を低下させるが、NMN処理はその影響から細胞を保護する。SIRT1をsiRNAで除去すると、tbuoohによる酸化ストレスに対するNMNの保護効果が著しく低下する。これを示すために、研究チームはマウスのSIRT1発現を除去した(右の棒グラフ)。さらに、マウスの遺伝子を抑制するために非特異的で非機能的な混合物を用いた(左の棒グラフ)。酸化ストレスの下では、NMNはSIRT1の細胞生存率を著しく向上させたが(左から3番目のコラム)、SIRT1はその影響を排除した(右から3番目のコラム)。以上の結果から、酸化ストレス後の光受容体の保護にはSIRT1の機能が必要であることが示された。
Vavvas氏らは、「私たちの研究は、NMN(NAD+を促進する分子)が網膜脱離による光受容体の変性に対して神経保護作用を持つことを裏付けた」と述べた。研究者らは、NMNが酸化ストレスを減少させ、抗酸化HO-1レベルを増加させることで光受容体の細胞死を抑制することで神経炎症を緩和し、さらに網膜を保護すると考えている。
光受容体細胞に対するNMNの保護作用の将来の研究
これらの結果が加齢に伴う眼疾患の治療に応用できるようになるまでには、NMNの光受容体細胞保護効果が人に適用できるかどうかを見極める臨床研究が必要である。そうであれば、NMNの補充は糖尿病性網膜症や黄斑変性、網膜脱離などの患者さんの視力を守るのに希望をもたらすかもしれない。
Story Source
Chen X, Amorim JA, Moustafa GA, Lee JJ, Yu Z, Ishihara K, Iesato Y, Barbisan P, Ueta T, Togka KA, Lu L, Sinclair DA, Vavvas DG. Neuroprotective effects and mechanisms of action of nicotinamide mononucleotide (NMN) in a photoreceptor degenerative model of retinal detachment. Aging (Albany NY). 2020 Dec 29;12. doi: 10.18632/aging.202453. Epub ahead of print. PMID: 33373320.
