Newsお知らせ
NMNなどの分子は網膜のエネルギー生成を改善することで加齢黄斑変性を緩和する
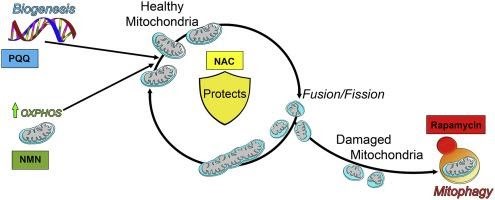
上図は加齢黄斑変性眼球細胞で試験された4種類の分子の機能を示す。NACは、ミトコンドリアを保護し、元気なミトコンドリアを増やす。ラパマイシンは、ミトファジーと呼ばれるプロセスの刺激により欠陥のあるミトコンドリアを除去する。PQQは、生物発生というプロセスを経てミトコンドリアの生成を刺激する。NMNは、酸化的リン酸化というプロセスを経てアデノシン三リン酸(ATP)と呼ばれるエネルギーのもとを増やす。
加齢黄斑変性(age-related macular degeneration: AMD)は、成人の視力低下の主な原因となっており、先進国では75歳以上の100人に20~30人が発症している。AMDは、網膜の中心部にある小さな黄斑の変性によって生じ、視野の中心で失明を引き起こす。
AMD患者は、文字が読みにくい、人の顔が識別できない、日常生活に支障が出てしまう。現在行われているAMD治療法は、目の中心部に血管が発達している萎縮型(ドライタイプとも呼ばれる)AMD患者の約10%しか治療できない。残りの90%の滲出型(ウェットタイプとも呼ばれる)AMD患者は、網膜(目の光に敏感な組織である)の細胞がなくなるため、現在のところ彼らへの利用可能な治療法がない。
過去の研究では、細胞のエネルギーのもとであるミトコンドリアの欠陥がAMD疾患の鍵を握っていることが示されていたと考えた上に、科学者らはそれを標的にして萎縮型のAMDに立ち向かいた。2020年5月号のRedox Biology誌に掲載されたミネソタ大学眼科の研究では、N-アセチル-L-システイン(N-acetyl-L-cysteine: NAC)、ラパマイシン(Rapamycin)、ピロロキノリンキノン(Pyrroloquinoline quinone: PQQ)、ニコチンアミドモノヌクレオチド(Nicotinamide mononucleotide: NMN)という4種類の分子で、AMD患者におけるミトコンドリアの機能不全を治療させたことが明らかになった。異なるAMD患者の細胞が薬物毎に異なる反応を示したことは、AMD患者への個人化治療法の開発という可能性があることを示唆している。言い換えれば、特定の患者に効く治療法と効かない治療法があるため、臨床医は、個々の患者に最も効果的な治療法を評価することができるということである。
研究者グループは、ミトコンドリアへの効果により4種類の分子を選んだ。NACは、ミトコンドリアを酸化ストレスから守り、細胞内のエネルギーのもとであるアデノシン三リン酸(ATP)分子を生成するミトコンドリアの数を増加させることで、ATPを増やさせる。また、PQQは強力な分子であり、ミトコンドリアの生成を刺激することで細胞内のミトコンドリア量を増加させる働きがあると研究者らも認識している。ミトコンドリアの数を増加させる以外に、ラパマイシンを用いてマイトファジーと呼ばれるプロセスで細胞に欠陥のあるミトコンドリアの除去を誘導すると、さらにミトコンドリアの機能も改善される。NMNは、ニコチンアミドアデニンジヌクレオチド(NAD +)分子の濃度を高め、細胞のエネルギー生産や細胞の健康を促進する。
ミトコンドリアは、酸化的リン酸化と呼ばれるプロセスを経てATPを生成し、全身のエネルギーのもととなる。ATPレベルを測定することにより、科学者はミトコンドリアの機能を評価することができる。この4種類の分子による細胞の治療は、ミトコンドリアの機能を改善したのは一部のAMD患者に過ぎなかった。ラパマイシン、PGG、NMNが患者の網膜細胞のATPレベルを大幅に増加させたが、NACが増加させなかった。
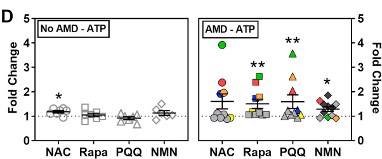
この4種類の分子は、ドナーの眼球細胞における一部の網膜色素上皮でのエネルギー生成を増加させる。左の枠は加齢黄斑変性のないドナーの細胞のデータを、右の枠は加齢黄斑変性のあるドナーの細胞のデータを示す。「変化倍率」とは、治療を行っていなかったエネルギー分子ATPレベル(1とする)との比率である。すべてではなく一部の患者は、ラパマイシン、PQQ、NMNにおいてATPのレベルアップが統計学的に明らかだ。
半数の患者の網膜細胞では、治療によりミトコンドリア機能が50%~350%改善されたが、残りの患者の網膜細胞ではミトコンドリア機能が5%~25%改善された。さまざまな患者の細胞は、分子に対して非常に個人化された応答を示す。
研究者らは「この研究結果は、AMD治療には個々の患者に合わせたアプローチが必要であるという考えを裏付けている。」と述べた。「事前に患者を選別する方案を開発し、最適なインターベンションタイプを確定することは、有効なAMD治療法を見つけるキーポイントである。」
出典
情報源:
Ebeling MC, Polanco JR, Qu J, Tu C, Montezuma SR, Ferrington DA. Improving retinal mitochondrial function as a treatment for age-related macular degeneration [published online ahead of print 2020 May 18]. Redox Biol. 2020;101552. doi:10.1016/j.redox.2020.101552.
参照論文:
1. Friedman DS, O’Colmain BJ, Muñoz B, et al. Prevalence of age-related macular degeneration in the United States [published correction appears in Arch Ophthalmol. 2011 Sep;129(9):1188]. Arch Ophthalmol. 2004;122(4):564-572. doi:10.1001/archopht.122.4.564.
2. Wong WL, Su X, Li X, et al. Global prevalence of age-related macular degeneration and disease burden projection for 2020 and 2040: a systematic review and meta-analysis. Lancet Glob Health. 2014;2(2):e106-e116. doi:10.1016/S2214-109X(13)70145-1.
